バーテックス、腎臓病治療薬の有望な後期段階の結果を受け、米国での承認を申請へ
Kamal Choudhury
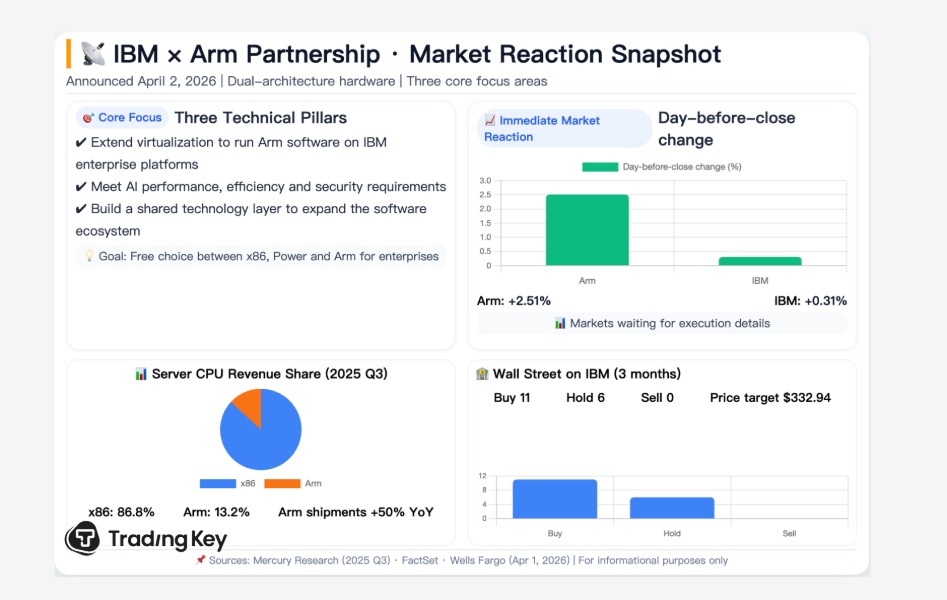
[ 3月9日 ロイター] - バーテックス・ファーマシューティカルズVRTX.Oは月曜日、同社の実験薬が後期臨床試験で腎臓障害の重要な徴候を激減させ、今月末までに米国での承認を求める軌道に乗ったと 発表した。
同社の株価は取引時間中に約7%上昇した。
ポベタシセプトは、IgA腎症患者の治療薬として開発されている 。この重篤な自己免疫疾患は、診断から20年以内に腎不全または死亡に至る患者の割合が多い、とバーテックス社は述べている。
本試験の中間データによると、ポベタシセプトは、プラセボを投与された患者では4.3%の減少であったのに対し、36週間後には腎臓障害の重要な徴候である尿中蛋白を52%減少させることができた。
BMOキャピタル・マーケッツのアナリストであるエヴァン・セイガーマンは、この結果について「ポベタシセプトはIgANにおける明確な競合薬であり、潜在的リーダーである」と述べた。
この薬剤はまた、プラセボと比較して有害な抗体のレベルを約79.3%低下させ、85%以上の患者で尿中の血液を除去するのに役立った。
このデータは、大塚製薬の4768.T 承認治療薬ヴォイザクト (link) に匹敵する有効性を示しており、ベラ・セラピューティクスの実験薬VERA.Oアタシセプトにも匹敵すると、シーガーマン氏は述べた。
バーテックス社によれば、この薬剤は4週間に1回注射で投与され、全般的に安全で忍容性も良好であったとのことである。
中間結果は36週間の治療を終えた199人の患者を対象としている。
605人の患者を対象とした完全な臨床試験は2年間継続され、本薬剤が長期的に腎機能の低下を遅らせるかどうかを測定する予定である。
バーテックス社は、3月末までに米国食品医薬品局への申請を完了する予定であり、優先審査バウチャーを利用して標準的な審査期間を10ヶ月から6ヶ月に短縮するとしている。