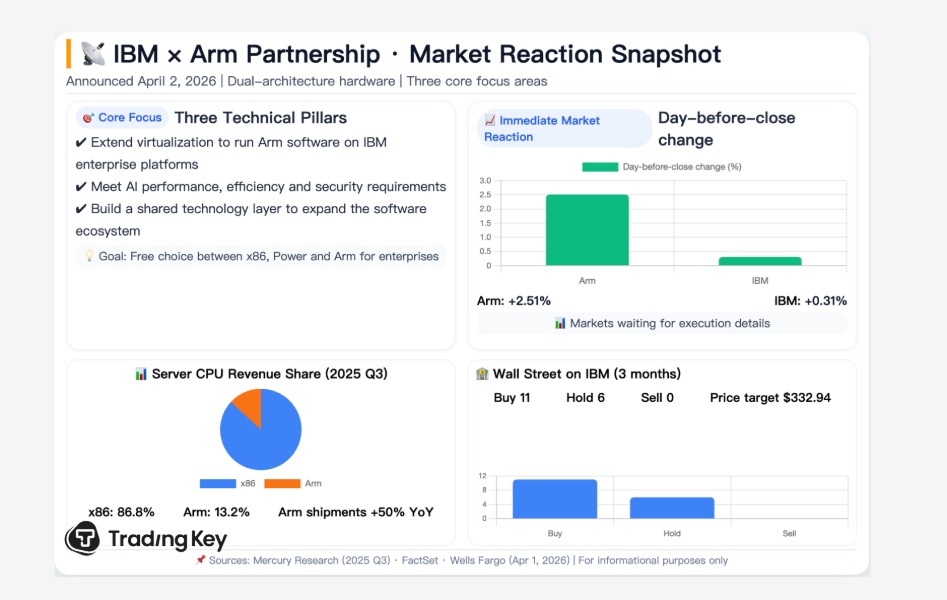
米FDA、ペプジェン社の筋疾患治療薬の臨床試験を一部保留
[ 3月4日 ロイター] - ペプジェンPEPG.Oは水曜日、米国食品医薬品局(FDA)が希少筋疾患治療薬の中間段階での臨床試験を一部保留にしたと発表した。これを受けて、同社の株価は延長取引で25%超急落した。
PGN-EDODM1は筋強直性ジストロフィー1型に対する試験薬で、時間の経過とともに筋肉が弱くなったり固くなったりする遺伝病で、運動や日常生活が困難になる。
ペプジェン社によれば、規制当局の懸念は同社が提出した以前の実験室および動物実験に関するものである。
当局は、初期段階の研究で得られた患者データからは安全性に関する懸念を指摘しなかった。
ペプジェン社によれば、FDAと協力してこの疑問に対処しており、初期の試験から新たに非盲検化されたデータを含む追加情報を提出する予定である。
米国での試験は保留されているが、同社は韓国、オーストラリア、ニュージーランド(NZ)での試験開始を承認されている。
英国とカナダでは、独立安全委員会からの用量漸増の勧告を受けて、すでに10mg/kgの用量で治療が行われている。
米国では、臨床保留措置が取られるまで、この試験に登録された患者はいなかった。
ペプジェン社によると、2025年12月31日現在、1億4850万ドルの現金と投資があり、27年後半までの事業運営に十分な資金があるという。
免責事項:本サイトで提供する情報は教育・情報提供を目的としたものであり、金融・投資アドバイスとして解釈されるべきではありません。