诺和诺德首款口服减肥药FDA获批!礼来霸主地位还能稳多久?
诺和诺德的口服Wegovy获FDA批准,成为首款GLP-1类口服减肥药,此举有助于其在美国市场份额争夺中抢占先机。该药物的推出旨在应对注射剂供应不足导致的市场份额流失,并与竞争对手礼来公司形成差异化竞争。临床试验显示,口服Wegovy平均可实现16.6%的体重降低,预计将吸引更多对注射存在顾虑的患者,推动全球减肥药市场增长。医疗从业者对口服剂型普遍持积极态度,预计将于1月初在美国上市。

TradingKey - 在与礼来公司的减肥药霸权争夺战中,诺和诺德终于迎来战略转折点!
12月22日周一,美国食品药品监督管理局(FDA)正式批准诺和诺德Wegovy注射剂的口服片剂版本,使其成为全球首款获批的GLP-1类口服减肥药。
这一突破不仅让诺和诺德抢在礼来口服减肥药奥福格列隆(orforglipron)获批之前占据市场先机,更在其经历股价腰斩、市场份额流失、盈利预警的至暗时刻,为公司注入一剂强心针。
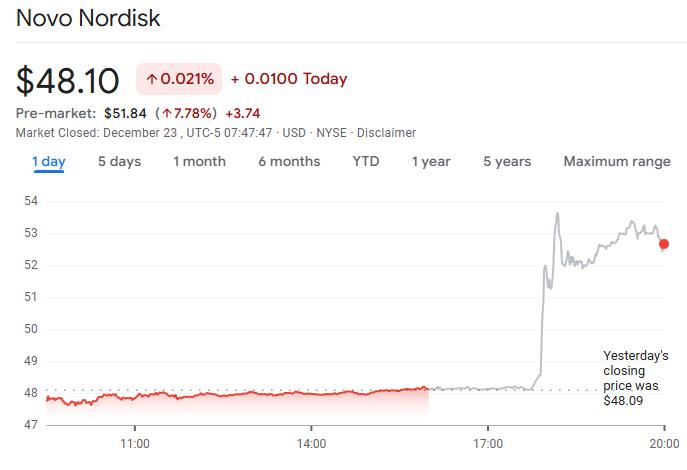
获批消息公布后,诺和诺德在美国上市的股票在盘前交易中上涨超7%。
重振市场份额的关键一役
美国公共卫生数据显示,全国约四成成年人面临肥胖困扰,而KFF最新民调揭示,当前约12%的成年人正在使用GLP-1类药物进行体重管理或慢性病治疗。这一庞大的患者群体,构成了制药巨头竞相争夺的核心战场。
对诺和诺德而言,2025年是充满挑战的一年,该公司的股价今年已累计下跌超过44%。
尽管其在注射型减肥药领域曾拥有先发优势,却因难以应对需求的爆炸式增长,导致市场份额被竞争对手蚕食。礼来公司凭借其注射剂Zepbound迅速反超,该产品不仅在疗效上被证明优于诺和诺德的Wegovy,更在美国每周处方量排行榜上占据领先地位。
在这一背景下,FDA对口服Wegovy的批准显得尤为关键。BMO Capital Markets分析师Evan Seigerman在报告中指出:"诺和诺德的GLP-1减肥药片获得批准,对于该公司而言,在最近面临维持肠促胰素市场份额主导地位的挑战之际,这无疑是一次急需的胜利。"
诺和诺德正寄希望于这款口服药丸的先发优势来重振其在美国市场的销售表现。礼来的下一代口服减肥药福格列隆最早可能在3月底获得批准,该时间窗口对诺和诺德至关重要。
诺和诺德美国运营执行副总裁David Moore表示,每日服用的药丸可能会提高人们对该药物的兴趣和使用率。他透露,公司正在美国北卡罗来纳州生产这款药丸,并且"一段时间以来"一直在储备该药丸的供应,以确保"充足的供应"。
面对全球医疗体系因肥胖问题而承受的日益增长的经济负担,这种口服疗法有望覆盖更广泛的治疗需求,为数千万尚未得到有效干预的患者提供新方案,预计将在2030年代推动全球减肥药市场规模达到每年1500亿美元的水平。
从注射到口服的跨越
一些健康专家表示,口服剂型的问世将为两类特定人群带来福音:一类是对注射存在心理抵触的患者,另一类则是那些认为自身状况尚未严重到需要接受注射治疗的潜在获益者。
远程医疗公司Ro的首席执行官Zachariah Reitano称:“有些人害怕打针,有些人会出现‘注射疲劳’,还有些人觉得自己病情不严重,认为注射治疗过于激进,对他们而言,口服药物无疑是更便捷的选择。”
诺和诺德公司表示,口服药片含有25毫克司美格鲁肽,与注射用Wegovy和Ozempic的活性成分完全一致,将继续以“Wegovy”为品牌名称进行销售,并计划于1月初在美国开始销售这款新药片。
Oasis 4三期临床试验的结果为该药物的临床价值提供了坚实依据。数据表明,每日服用25毫克剂量的患者,在64周的治疗周期后,平均体重降低了约16.6%,减重效果显著。
医疗从业者的接受度调查显示,医生群体对口服剂型展现出高度认可。FirstWord近期针对美国和欧洲内分泌科及全科医生的调研发现,85%的受访者表示至少会在某种程度上优先选择开具口服Wegovy而非注射剂。
诺和诺德美国运营执行副总裁Dave Moore在获批前表示:"我们通过多年的研究发现,口服药物的出现确实能够吸引、激活并激励不同人群寻求治疗。他们可以与医生讨论这种药物是否适合自己。"
"我们感到兴奋的是,能够为人们提供另一种选择,并确保他们能够像使用注射剂一样便捷地获得治疗,"他继续说道。













